肿瘤细胞的保护性自噬及其DNA损伤修复是肿瘤治疗耐受的重要原因,放射医学与辐射防护国家重点实验室、医学部放射医学与防护学院分子影像与核医学研究中心发现Au@Cu2-xSe纳米颗粒抑制脑胶质瘤细胞保护性自噬和DNA损伤修复增强放疗疗效的新机制。相关成果以“Inhibiting autophagy flux and DNA repair of tumor cells to boost radiotherapy of orthotopic glioblastoma”为题发表在Biomaterials杂志上(Biomaterials 280 (2022) 121287)。论文链接:https://doi.org/10.1016/j.biomaterials.2021.121287。
放疗是脑胶质瘤治疗的常用手段。然而,放疗使肿瘤细胞产生保护性自噬,降低对其DNA的持续性损伤,导致脑胶质瘤产生很强的放疗耐受,克服放疗耐受对提高其放疗效果具有重要意义。在前期工作中,分子影像与核医学研究中心团队构建了“大成若缺、富含空位”的Cu2-xSe超小纳米颗粒。这种纳米颗粒具有丰富的内在新颖性质,如光热、光动力、化学动力、放射增敏等,不仅可用于肿瘤的成像和治疗(Adv. Mater. 2016, 28, 8927–8936;Nano Lett, 2018, 18, 4985-4992;Nanoscale, 2019, 11, 7600–7608; ACS Appl. Mater. Interfaces 2019, 11, 16367−16379;Adv. Funct. Mater. 2020, 30, 1906128;Adv. Funct. Mater. 2021, 202108971);而且还可用于帕金森疾病的治疗(J. Am. Chem. Soc. 2020, 142, 21730−21742)。为了增强Cu2-xSe纳米颗粒的成像和治疗效果,研究团队还对其进行功能化,显著提高其诊疗效果(ACS Nano, 2017, 11, 5633-5645; ACS Nano, 2019, 13,1342-1353; ACS Appl. Mater. Interfaces 2020, 12, 4231−4240)。
在上述研究基础上,本研究构建了具有核壳结构的Au@Cu2-xSe纳米颗粒,通过抑制肿瘤细胞保护性自噬,降低放疗引起的DNA损伤修复,从而提高脑胶质瘤的放疗效果。研究发现Au@Cu2-xSe 纳米颗粒一方面通过改变肿瘤细胞溶酶体的酸碱度,有效抑制自噬流,促使其SQSTM1/p62蛋白水平上调;另一方面,它们促进DNA损伤修复的关键蛋白Rad51泛素化,使其被蛋白酶体系统降解,阻碍放疗过程中的DNA损伤修复。纳米颗粒通过同时抑制放疗引发的保护性自噬及DNA损伤修复,明显抑制原位脑胶质瘤生长,显著提高了放疗疗效。该研究为合理设计用于抑制肿瘤细胞保护性自噬和DNA损伤修复增强疗效的纳米颗粒提供了新思路。
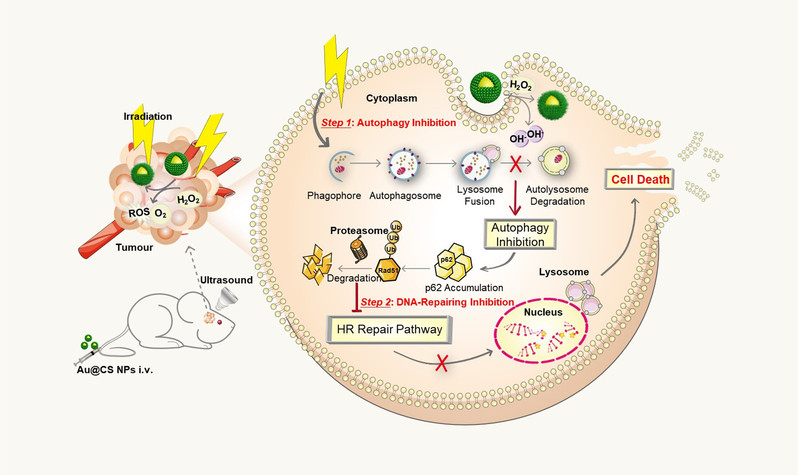 图1. Au@Cu2-xSe纳米颗粒抑制肿瘤细胞自噬流、阻碍DNA损伤修复及提高放疗敏感性的示意图
图1. Au@Cu2-xSe纳米颗粒抑制肿瘤细胞自噬流、阻碍DNA损伤修复及提高放疗敏感性的示意图
放射医学与辐射防护国家重点实验室、医学部放射医学与防护学院为论文第一单位,论文第一作者为苏州大学放射医学与防护学院的硕士生许琦,张浩博士和李桢教授为该文章的通讯作者。该研究得到了国家自然科学基金(81971671),国家重点研发计划(2018YFA0208800),江苏省重点研发计划(BE2019660)等项目的支持。